

走进南宫28
NEWS南宫28:ofCS成CTC多癌种检测新靶标,推动癌症早筛技术创新
来源:汪晓彬 日期:2025-07-19癌症早期诊断与精准治疗始终是生物医疗研究的重要课题。作为一种非侵入性检测技术,液体活检通过分析循环肿瘤细胞(CTCs)、细胞外囊泡和循环肿瘤DNA(ctDNA)等血液生物标志物,实现了对肿瘤的早期诊断、预后评估和疗效监测。其中,CTCs被誉为癌症转移的“前哨细胞”,它们携带着肿瘤的表型和基因型信息,是研究最为广泛的液体分析物之一。然而,由于CTCs在血液中的丰度极低及其高度的异质性,传统检测技术在癌种特异性和细胞表型变异上面临诸多限制,尤其是针对非上皮来源或低表达上皮标志物的CTCs检测效果较差,导致其在临床应用中面临显著挑战。
近期,一项名为“Multi-cancer detection of circulating tumor cells by targeting oncofetal chondroitin sulfate”的研究成果,发表于npj Precision Oncology期刊。该研究提出了一种基于靶向癌胚硫酸软骨素(Oncofetal Chondroitin Sulfate, ofCS)的泛癌种CTCs检测技术,通过特异性识别肿瘤细胞表面的糖基化修饰,实现了对多种实体瘤(包括上皮和非上皮来源)的高效检测,从而为多种癌症的早期诊断与个体化治疗提供了新型生物标志物和更易操作的检测方法。
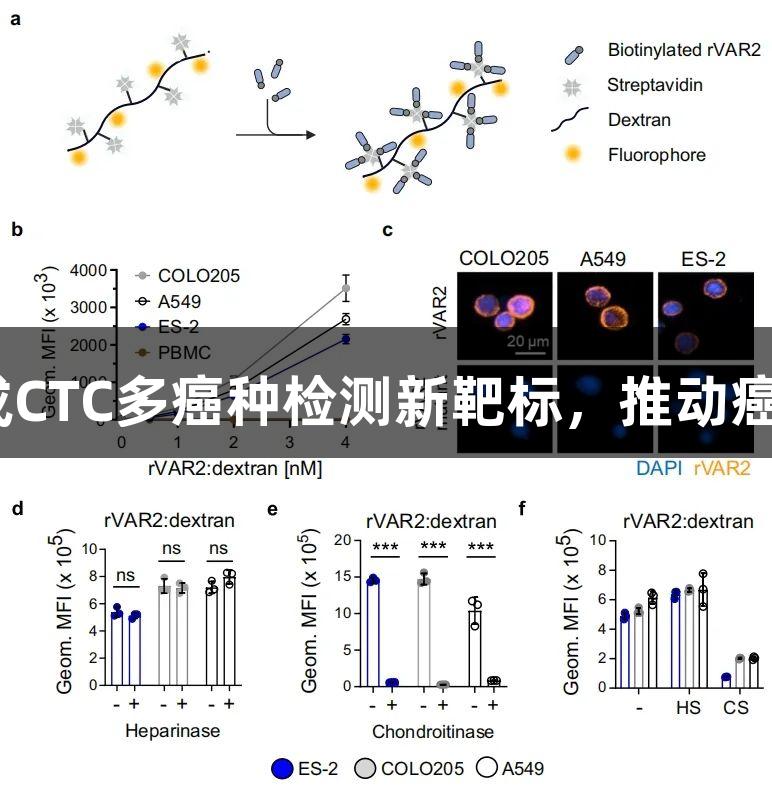
研究发现癌胚硫酸软骨素(ofCS)在多种恶性肿瘤中表现出高表达,而在正常成人组织中几乎没有表达,这一特性使其成为CTCs检测的理想分子标志物。研究团队运用化学偶联技术,将生物素化的疟原虫蛋白rVAR2(ofCS特异性结合配体)与携带多个链霉亲和素分子和荧光标记的聚合物联接,提高了rVAR2的亲和力,同时增强了荧光信号,成功构建了高灵敏度、高特异性的CTCs检测探针。
通过分子动力学模拟和结构生物学分析,研究团队优化了rVAR2与聚合物的偶联方式,提高了探针在复杂血液环境中的稳定性和结合效率。实验结果显示,优化后的探针对ofCS阳性CTCs展现了高度特异性,而对健康供体PBMCs的结合则极低。进一步的实验通过突变体对照与酶解实验证明了这一结合特异性是由癌细胞表面硫酸软骨素(CS)介导,且rVAR2的结合与细胞系的EpCAM或CK状态无关。
为了验证rVAR2-聚合物对癌细胞与PBMC的特异性,研究团队将癌细胞掺入健康人血样,并通过荧光标记法进行检测。结果显示,平均癌细胞回收率超过50%,且不受参与细胞数量影响,表明该方法对CTCs检测具有高灵敏度与可靠性。
为评估rVAR2-聚合物染色法在CTCs检测中的临床适用性,研究团队在两个不同患者队列中进行了测试。结果显示,在25名患有上皮癌症的患者中,有24%检测到ofCS+ CTC,而在3名非上皮癌症患者中,100%检测到了ofCS+ CTC。此外,在健康捐献者的血液样本中未检测到ofCS+细胞,证明了rVAR2-聚合物染色法的癌症特异性。
基于rVAR2-聚合物探针的多癌种CTCs检测技术展示了其在癌症早期诊断上的巨大潜力,突破了传统方法的癌种限制,显著提高了多种癌症环境中的临床效用。这一高灵敏度与特异性的检测方法为癌症的早期干预提供了关键的时间窗口,有助于在肿瘤可治愈的阶段发现病变,并推动个体化治疗的发展。
在这一研究中,南宫28的细胞成像多功能微孔板检测仪发挥了主要技术支持作用,提供了高分辨率成像、自动化扫描和多通道荧光分析等功能,助力癌症研究的开展。随着技术的进步,南宫28将继续在科研攻坚中为研究者提供强有力的支持。
如需了解更多信息,欢迎关注南宫28!
全国客户服务热线
13898611727
总部地址:上海南长区薛街道88号